Μάθημα : Φυσικοχημεία Ι (E 2024-25)
Κωδικός : CHEM105
11414 - Αθανάσιος Τσεκούρας
Ημερολόγιο
Μάιος 2025 | |
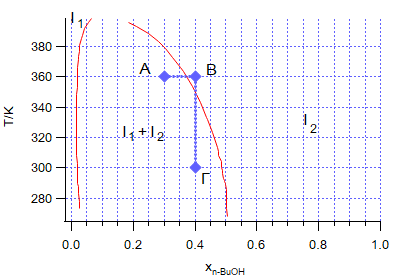
| Ωσμωτική πίεση, μερική διαλυτότητα υγρών, σημεία τήξεως μιγμάτων (Διάρκεια: 2:00 ώρες) Τρίτη 20 Μαΐου 2025 - 9:15 π.μ. Εξετάσαμε το φαινόμενο της ωσμώσεως και καταλήξαμε στην σχέση της ωσμωτικής πιέσεως. Συζητήσαμε τις ισορροπίες υγρών τα οποία δεν μπορούν να σχηματίσουν μίγματα σε οποιαδήποτε αναλογία. Είδαμε την εξάρτηση των συνθηκών ισορροπίας των διαφορετικών υγρών φάσεων από την θερμοκρασία. Μελετήσαμε την συμπεριφορά του σημείου πήξεως υγρών μιγμάτων σε μεγάλο εύρος τιμών γραμμομοριακού κλάσματος και διαπιστώσαμε την υπάρξη ευτηκτικού σημείου. Καταγραφή διαλέξεως: 1η ώρα, 2η ώρα Βιβλιογραφία: Άσκηση 29. Ποια είναι η διαφορά ωσμωτικής πιέσεως μεταξύ δύο υδατικών διαλυμάτων NaCl συγκεντρώσεων 0.1 mol/L και 0.2 mol/L σε θερμοκρασία 37 °C; Άσκηση 30. Στο σχήμα φαίνεται η αμοιβαία διαλυτότητα βουτανόλης και νερού σε διάφορες θερμοκρασίες. Αν τοποθετήσουμε σε ένα δοχείο 3 mol βουτανόλης και 7 mol νερού σε 360 K, πόσες φάσεις θα σχηματιστούν και με τι σύσταση η καθεμιά; Ποια ουσία και σε τι ποσότητα πρέπει να προστεθεί στο σύστημα για να φτάσουμε στο σημείο Β;
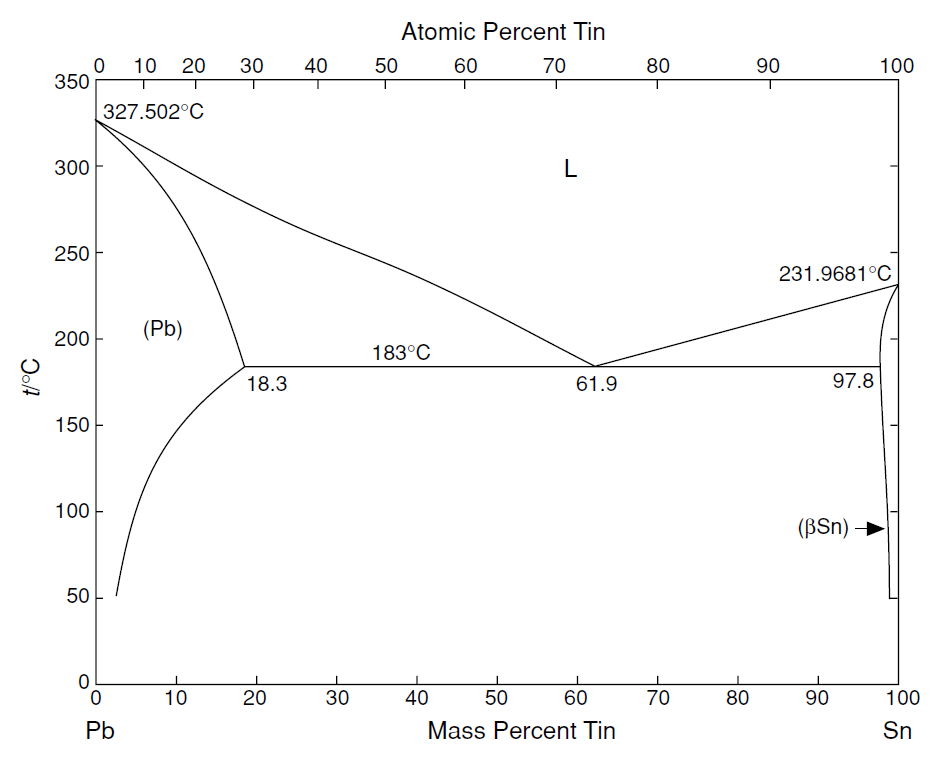
Άσκηση 31. Δίνεται το διάγραμμα σημείων τήξεως κραμάτων μολύβδου και κασσιτέρου. Σε ποια θερμοκρασία αρχίζει να πήζει κράμα με περιεκτικότητα κατά αριθμό 40%; Τι στερεό σχηματίζεται; Αν η θερμοκρασία μειωθεί σε 200 °C, τι στερεό σχηματίζεται και ποια είναι η αναλογία μαζών στερεού και υγρού σε εκείνο το σύστημα;
|